
Par le Dr Solène MORANT
Le « dysraphisme spinal » du braque de Weimar
Le « dysraphisme spinal » du braque de Weimar est une maladie génétique très particulière décrite uniquement dans cette race. Cette maladie neurologique, d’origine génétique, est caractérisée par un phénotype clinique unique et non évolutif qui se traduit par une démarche en « saut de lapin » pathognomonique sur les membres pelviens mais qui ne nuit pas à la bonne qualité de vie du chien. Les quatre signes cliniques sont identifiables dès l’âge de trois à quatre semaines : « bunny hopping » ou démarche en saut de lapin, position « accroupie » spécifique, augmentation du polygone de sustentation et déficit proprioceptif au niveau des membres pelviens. On notera que le « dysraphisme spinal » du braque de Weimar n’est pas un vrai dysraphisme, en effet le terme « dysplasie spinale » semble plus approprié.

Le développement d’un test génétique
Le « dysraphisme spinal » du braque de Weimar est une affection neurologique connue depuis les années cinquante mais ce n’est qu’en 2013 que les travaux du Docteur Noa Safra ont permis d’identifier son support génétique : une mutation autosomique récessive du gène homéotique NKX2-8.
Dans ce travail de thèse, nous avons confirmé que les cas français étudiés étaient bien porteurs de la même mutation que celle identifiée aux États-Unis. D’autre part, via le dépistage effectué sur 88 braques de Weimar cliniquement indemnes, nous avons identifié huit individus porteurs, évaluant ainsi la prévalence de la version allélique mutée du gène NKX2-8 à 9 %. Ainsi, cette mutation reste rare mais ne peut cependant être négligée, notamment car la population de braques de Weimar française est relativement limitée, avec 1431 animaux seulement inscrits au L.O.F en 2019 (www.centrale-canine.fr).
Bien que les signes cliniques soient très pathognomoniques, face à un braque de Weimar suspect d’être atteint, il n’existe aucun autre outil diagnostic en dehors de l’examen histologique post-mortem. Le test génétique permet ainsi, grâce à un simple écouvillon buccal ou à une prise de sang sur tube EDTA, d’établir un diagnostic de certitude.
Conseil aux éleveurs
La fréquence de l’allèle morbide étant inférieure à 10 %, il est recommandé́ d’exclure les animaux hétérozygotes de la reproduction afin dans un premier temps, de limiter la propagation de l’allèle muté et dans un deuxième temps, d’éliminer cette mutation du patrimoine génétique de la race. Cependant, il est important de considérer à la fois le faible nombre de chiens inscrits au L.O.F et le fait que nous ne connaissons pas la distribution des hétérozygotes au sein des différentes lignées qui composent la race. En effet, le fait d’appliquer cette politique pourrait réduire certaines lignées à néant et reviendrait également à utiliser un nombre restreint de chiens pour la reproduction, ce qui appauvrirait inévitablement la diversité génétique de la race. D’autres anomalies d’origine génétique, non prises en compte lors du choix des reproducteurs, pourraient alors voir leur fréquence augmenter.
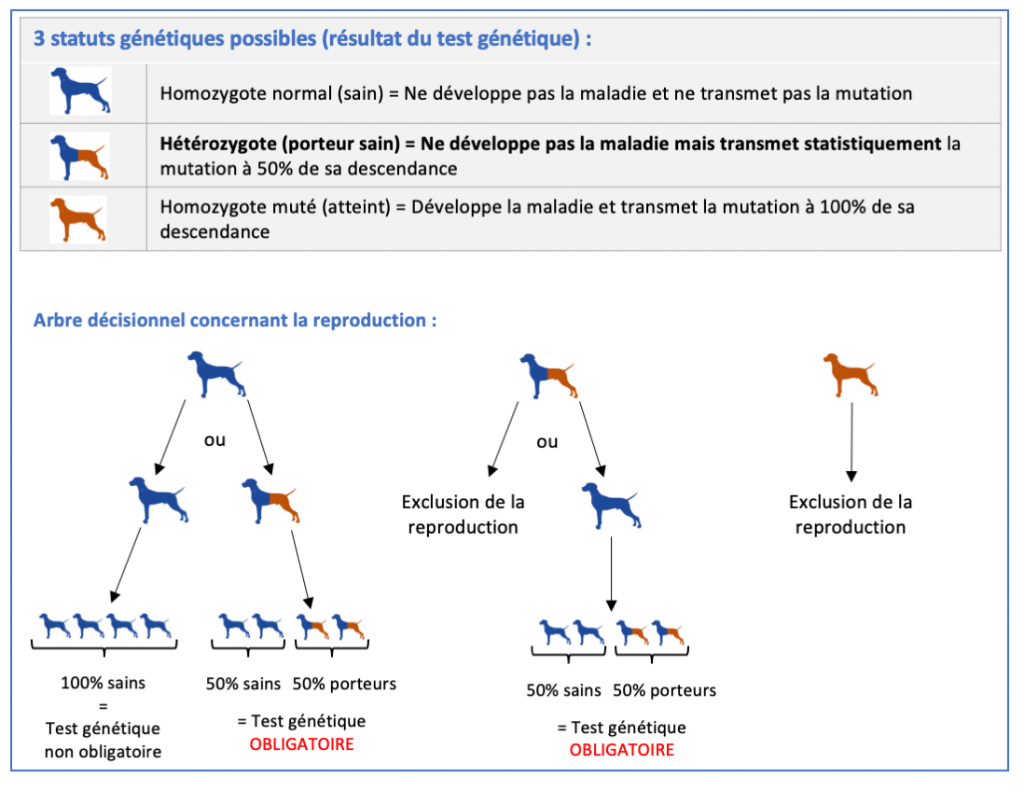
Arbre décisionnel concernant la reproduction du braque de Weimar, en fonction du statut génétique.
L’élimination de l’allèle muté peut se faire progressivement, en conservant certains hétérozygotes pour la reproduction. Il est cependant nécessaire de leur choisir des partenaires homozygotes sains. De plus, les chiots issus de ces accouplements devront être testés génétiquement s’ils sont destinés à la reproduction, car, statistiquement, 50 % d’entre eux seront hétérozygotes porteurs sains.
L’utilisation d’un homozygote muté (mâle ou femelle) comme reproducteur est à proscrire, car celui-ci ne peut engendrer que des descendants atteints ou porteurs sains (Figure).
Télécharger le manuscrit du Dr MORANT :
Référence
Safra N, Bassuk AG, Ferguson PJ, Aguilar M, Coulson RL, Thomas N, et al. Genome-wide association mapping in dogs enables identification of the homeobox gene, NKX2-8, as a genetic component of neural tube defects in humans. PLoS Genet. 2013;9(7):e1003646.
Publié le 3 Août 2020